据最新一期《自然·生物技术》杂志报道,澳大利亚默多克儿童研究所领导的研究团队在实验室中成功制造出与人体组织高度相似的造血干细胞。这一突破性进展有望为白血病及骨髓衰竭患者提供全新的个性化治疗路径。
长期以来,在实验室环境下培育出能够移植至动物模型、并能稳定生成健康血细胞的人类血液干细胞,一直是科学界面临的重大挑战。如今,该研究团队开发出一套创新工作流程,成功创建出与人类胚胎血液干细胞特性极为接近的可移植细胞。尤为关键的是,这些干细胞能够在符合临床要求的规模与纯度下进行培养。
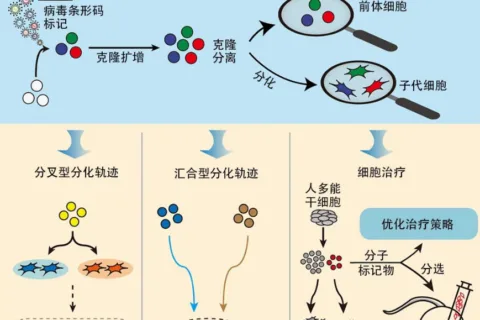
该技术始于将人类血液或皮肤细胞进行“重编程”,转化为多能干细胞。在此过程中,通过暂时激活四个特定基因,使细胞回归至发育早期阶段,从而获得分化为体内任何类型细胞的潜力。
研究人员随后将这些多能干细胞定向诱导为血液干细胞。通过培养悬浮于液体培养基中的细胞球(每个球体包含数百个细胞),约两周后,干细胞即可分化为血管细胞,并进一步产生数百万计的血细胞。
在后续实验中,这些实验室培育的血细胞被注入免疫缺陷小鼠体内。结果显示,约50%的细胞成功转化为功能性骨髓组织,能够生成与健康人类骨髓相同的携氧细胞与免疫细胞。这种长期稳定产生全部血细胞类型的独特能力,证实了这些细胞可作为真正的血液干细胞。
研究还证实,实验室培养的干细胞在移植前可进行冷冻保存,这一过程模拟了临床移植前供体干细胞的保存流程,为未来实际应用提供了重要技术支持。
造血干细胞移植常被视为血液病患者的“生命重启”,然而,配型难题始终困扰着众多患者。这项新技术的意义在于,未来或可直接利用患者自身的细胞(如皮肤细胞),将其重编程为干细胞后,再定向分化为所需的血液细胞进行移植,从而极大降低排异风险,改善治疗效果。
研究人员强调,此项研究标志着血液系统疾病治疗领域取得了里程碑式进展。但在最终应用于临床治疗前,仍需开展大量的人体试验以验证其安全性与有效性。