4月13日,国际顶级学术期刊《自然》发布了一项干细胞领域的革命性成果——通过化学小分子实现人体细胞命运的精准重编程,成功将人类成体细胞转化为具备多向分化潜能的干细胞。
这项突破性研究由北京大学生命科学学院、北大—清华生命联合中心邓宏魁教授领衔的团队完成。其核心在于,仅需在人类皮肤细胞的培养体系中添加特定的几种化学小分子组合,经过约一个月的诱导,皮肤细胞即可逆转为多潜能干细胞。此类干细胞拥有发育成人体所有已知细胞类型的巨大潜力,为再生医学打开了全新的大门。
回溯2012年,诺贝尔生理学或医学奖授予了“体细胞重编程技术”。然而,当时依赖转录因子(一种基因物质)的重编程方法存在效率偏低、潜在致癌风险以及技术可控性不足等局限,这些因素严重阻碍了其走向临床应用的进程。
为了攻克这些难题,实现更安全、更高效的干细胞制备,北京大学干细胞研究中心主任邓宏魁教授团队历经十余年不懈探索,致力于寻找能够逆转细胞命运的化学钥匙。他们的目标明确:运用纯粹的化学小分子,将已分化的人类体细胞“返老还童”,重编程为多潜能干细胞。
化不可能为可能:四步走策略实现精准诱导
多潜能干细胞通常源自早期胚胎,具备近乎无限的发育潜能。在生物技术介入之前,从胎盘、脐带等组织获取干细胞的方式较为初级,且所得干细胞的发育能力有限。
为了能够按需、便捷地获取干细胞,关键在于发展先进的制备技术,引导已分化的人类成体细胞逆向回归到干细胞状态。
“人类成体细胞的特性与稳态调控机制极为复杂,远超其他实验模型物种。”邓宏魁教授指出,这使得它们对外源化学小分子的刺激反应并不敏感。
这好比试图让一位全副武装的将军卸下装备,仅凭温和的劝说难以奏效。因此,科学界曾普遍认为,人类成体细胞受到极其严格的表观遗传限制,通过化学重编程激发其多潜能性几乎是一项不可能完成的任务。
为了将不可能变为现实,研究团队必须另辟蹊径。他们从低等动物的强大再生能力中获得灵感。“我们观察到,像蝾螈这样的低等动物在肢体受损后能够再生,这个过程涉及一个可塑的中间状态。”邓宏魁教授向媒体解释道,“这启发我们,细胞的重编程或许并非一步到位,而是可以分步实现的。”
基于这一创新思路,团队将研究重点转向构建一个关键的“可塑性中间态”,以此作为细胞逆分化的“跳板”。沿着这个方向,团队进行了海量化合物的筛选与组合测试。最终发现,高度分化的人成体细胞在特定化学小分子组合的作用下,确实能够发生类似去分化的现象,进入一种具有可塑性的中间状态。
“我们尝试了超过20种不同策略,筛选了上百万种化学小分子组合。”邓宏魁教授回忆道,仅为了找到合适的6个小分子组合,完成从成体细胞到可塑性中间态细胞这前半程转变,团队就耗费了整整六年时间。
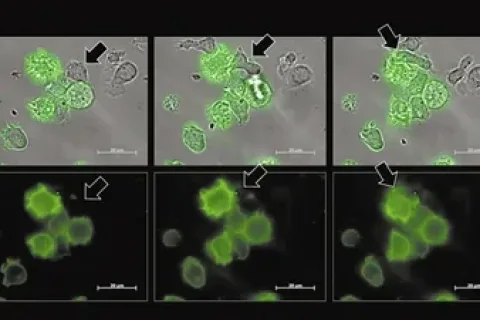
研究论文中的示意图清晰展示了这一过程:人类成纤维细胞首先转变为“可塑性中间态”细胞,随后干细胞特性逐步显现,最终成功通过化学小分子诱导出人多潜能干细胞。
化学小分子诱导:更简易、更安全、更高可控
“这项技术使得可控、高效地制备人体干细胞变得像服用一片阿司匹林那样简便。”美国萨尔克研究所的胡安·巴尔蒙蒂教授对此评价道,“它不涉及基因层面的操作,完全通过化学小分子实现,这将极大加速干细胞技术在重大疾病治疗中的应用,推动其迈向临床的进程。”
与传统技术相比,化学小分子诱导干细胞展现出多重显著优势:更高安全性、更简易的操作流程、易于标准化和精准调控。而这些正是原有技术难以克服、阻碍其临床转化的核心瓶颈。
在安全性方面,此前在小鼠模型中的实验已证实,化学诱导产生的干细胞所携带的遗传突变显著少于传统方法,并且由这些细胞形成的嵌合体小鼠在长达6个月的观察期内全部健康存活,未出现肿瘤。此外,由该干细胞分化得到的胰岛细胞移植到小鼠及非人灵长类动物模型体内后,长期观察也未发现肿瘤生成。
不仅如此,化学小分子诱导技术在个体化定制、细胞制备标准化方面同样优势突出。其操作简单,时空调控性强,作用过程可逆,小分子化合物易于合成与储存,所有这些特性都使其更易于进行标准化、规模化生产。
据悉,邓宏魁教授团队已利用化学诱导产生的干细胞,成功分化出功能性的胰岛细胞,并在非人灵长类动物模型中验证了其治疗潜力,为未来治疗糖尿病等重大疾病带来了新的希望。