近日,中国科学院、深圳华大生命科学研究院等机构的研究团队,在体外成功诱导出相当于受精卵发育3天状态的人类全能干细胞。这是目前全球范围内在体外培养的“最年轻”的人类细胞,标志着再生医学领域在人类多能干细胞研究之后,取得了又一里程碑式的进展。相关成果已于北京时间3月22日在国际顶级学术期刊《自然》(Nature)正式发表。
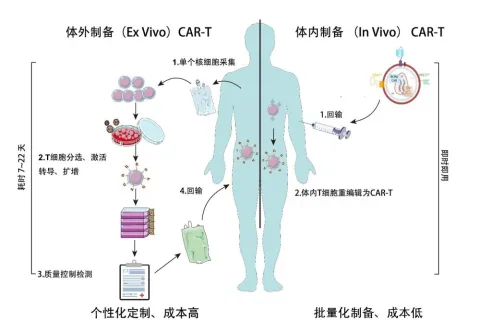
据悉,研究团队开发了一种非转基因、快速且可控的“鸡尾酒”细胞重编程方法,能够将人多能干细胞转化为具有全能性的8细胞期胚胎样细胞。该成果对于推动未来人体器官的体外再生,解决器官来源短缺、移植排斥反应等关键问题,具有重大意义。
回溯2012年,诺贝尔生理学或医学奖授予了成功将成熟体细胞诱导为囊胚阶段多能干细胞的日本科学家山中伸弥。人类囊胚期细胞相当于受精卵发育5至6天的状态,其后续发育潜能存在一定局限。
而本次研究则将该领域向前推进了一大步,首次在体外获得了相当于受精卵仅分裂3天的胚胎细胞。在胚胎发育早期,细胞状态日新月异,正是这关键的2至3天时间差,使得科学家首次通过体外诱导获得了人类8细胞期胚胎样全能干细胞。这是迄今体外诱导获得的最具发育潜力的“最年轻”人类细胞,也将为破解人类胚胎早期发育的奥秘提供全新钥匙。
据介绍,这些全能性的8细胞期胚胎样细胞,重现了受精卵分裂3次后的胚胎状态。与以往的多能干细胞相比,此类细胞具备分化为胎盘组织的潜能,并有望发育成更为成熟的各类体细胞组织。
“此项突破也是再生医学与前沿单细胞测序技术深度融合的典范。”论文通讯作者之一、深圳华大生命科学研究院刘龙奇博士表示,“通过大规模单细胞多组学图谱技术,对基于干细胞技术获得的细胞或组织进行高效鉴定与机制解析,将极大加速再生医学的临床转化进程。”
本研究首次在严格意义上实现了将人多能干细胞“逆向转化”为全能性胚胎细胞,使得已分化的“成年”细胞能够回归发育潜力更大的“婴儿期”状态。同时,由于获得的细胞更接近胚胎发育的原始起点,将其应用于再生医学领域,有望培育出形态与功能更接近天然器官的组织,从而提升移植的相容性与成功率。
这一突破的实现,离不开单细胞测序技术的持续进步。以往,研究人员往往需要对成千上万个细胞进行繁琐的培养与筛选,成功率不足10%。如今,依托华大自主开发的单细胞建库测序平台(DNBelab C4)与DNBSEQ测序技术,科学家能够以更高的灵敏度与准确性开展多维单细胞分析,快速锁定具有关键发育潜能的细胞,并追踪其后续发育轨迹。
研究过程中,团队还将诱导获得的全能干细胞注入小鼠体内进行后续发育,并利用华大的单细胞测序技术进行大规模细胞图谱分析。分析结果确认,实验所得的全能干细胞与人类8细胞期胚胎细胞高度相似,充分证明了其全能性。这为未来利用患者自身细胞培育器官,并用于个性化移植修复,奠定了坚实的科学基础。
本研究由中国科学院与深圳华大生命科学研究院主导,联合英国剑桥大学、吉林大学、孟加拉国拉杰沙希大学等多个国际团队共同完成。所有实验均通过严格的伦理审查,并遵循国际国内相关法规与伦理准则。