科技日报北京3月3日电 (记者冯卫东)双特异性抗体作为一种前沿的工程药物,能够同时识别并结合两种不同的肿瘤抗原,通过多靶点协同作用有效抑制肿瘤生长。近期,美国约翰·霍普金斯大学的三支研究团队分别成功研发出可同时结合肿瘤抗原与T细胞的双特异性抗体,为癌症的个性化免疫治疗开辟了新的技术路径。
首项研究成果发表于《科学》杂志。该团队设计的双特异性抗体能够特异性靶向突变型p53蛋白,同时避免对正常细胞中野生型p53的干扰。p53是关键的肿瘤抑制基因,在部分癌症中发生失活突变,传统药物难以重新激活其功能。
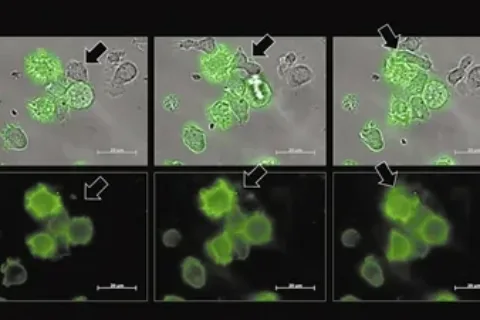
该抗体一端结合突变p53蛋白片段,另一端与T细胞相连。研究显示,在多发性骨髓瘤小鼠模型中,该抗体可有效激活T细胞,特异性清除携带突变p53的癌细胞,并显著抑制肿瘤进展。即使肿瘤细胞表面p53靶标表达水平极低,该抗体仍能介导强烈的T细胞抗肿瘤应答。
第二项研究发表于《科学·免疫学》。团队针对另一类难以靶向的致癌突变——RAS基因进行攻关。突变RAS蛋白通常表达量低,是肿瘤治疗中的经典难题。
研究人员首先开发了靶向RAS突变新抗原的抗体,进而将其构建成T细胞导向的双特异性抗体。在肺癌与胰腺癌患者来源的细胞系测试中,该抗体能精准清除低水平表达突变RAS的肿瘤细胞,而对仅表达正常RAS的细胞无影响。
第三支团队的研究聚焦于恶性T细胞特异性靶点,相关论文发表在《科学·转化医学》。其设计的双特异性抗体可靶向恶性T细胞表面的TRBV5-5或TRBV12区域。
在白血病与淋巴瘤的人源及小鼠模型细胞系中,该抗体能精准识别并清除驱动肿瘤的恶性T细胞,同时保护健康T细胞不受影响,并观察到肿瘤消退效应。
美国得克萨斯大学乔恩·魏丹兹博士在《科学》社评中指出,这些研究为开发“即用型”蛋白基癌症免疫疗法提供了新可能。不过他也提醒,在实现临床转化前,双特异性抗体仍面临诸多挑战需进一步攻克。