刚刚过去的6月,国家药监局宣布了10多个新药通过优先审批成功上市。
其中,国内首款细胞疗法产品——阿基仑赛注射液获批在业内关注度颇高,中国在细胞疗法产品上终于实现了“零的突破”。
作为深耕生物科技领域的创新企业,湖南元初生物持续关注着细胞治疗这一前沿领域的发展。此次国内首款产品上市,标志着我国在该领域迈出了关键一步,也为后续的创新研发注入了强劲信心。
细胞疗法因其高度的个体化定制特性,在研发与生产上与传统药物有显著不同。这也使得其成本构成复杂,市场定价备受关注。细胞治疗究竟是什么?其高昂成本的背后有哪些技术支撑?临床应用前景与风险如何?哪些患者群体能从中最大获益?我们试图从产业与技术的角度进行探讨。
价值与可及性:细胞疗法的定价逻辑与产业思考
首款CAR-T细胞治疗产品获批后,其可能的定价成为焦点。这背后反映的是创新疗法“高研发投入、个体化生产”带来的成本现实,以及让更多患者受益的可及性挑战。
复星凯特的阿基仑赛注射液(Yescarta)的获批,为中国复发或难治性大B细胞淋巴瘤患者提供了新的治疗选择。其在美国的定价曾引发广泛讨论。据悉,复星凯特方面表示,国内定价方案尚未最终确定,正在多方沟通中。
该疗法源于海外技术引进,其显著的临床数据是支撑其价值的基础。研究显示,对于特定淋巴瘤患者,该疗法能带来高缓解率,为部分难治患者带来了长期生存的希望。
然而,动辄百万的潜在治疗费用,确实构成了患者获得治疗的门槛。如何在激励企业持续创新、回收巨额研发与生产成本的同时,逐步提升创新疗法的可及性,是包括企业在内的整个产业生态需要共同面对的课题。有行业专家曾提出,寻找一个平衡各方诉求的“合理价格区间”,是推动技术惠及更多患者的关键。
“私人定制”的科技:解读细胞治疗的本质
要理解细胞疗法,首先要明白其“活细胞药物”和“个体化定制”的核心属性。
根据相关技术规范,细胞治疗通常指将来源于患者自体或异体的体细胞,经过体外特定的培养、扩增、激活或基因修饰等操作后,再回输到患者体内,以达到治疗疾病的目的。这个过程高度个体化,堪称“私人定制”的药物。
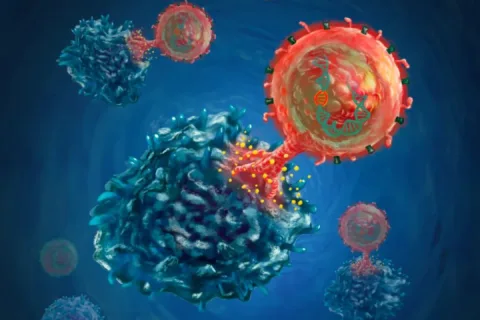
本次获批的阿基仑赛注射液属于CAR-T(嵌合抗原受体T细胞)疗法。其原理是采集患者自身的T细胞,在体外通过基因工程手段,为其装上能特异性识别肿瘤细胞表面抗原(如CD19)的“导航装置”——CAR(嵌合抗原受体)。这些被“武装”和扩增后的T细胞回输到患者体内后,便能精准识别并摧毁表达相应抗原的肿瘤细胞。
目前,CAR-T疗法在血液系统肿瘤(如某些淋巴瘤、白血病)中取得了突破性进展,这主要是因为血液肿瘤的靶点相对明确、均一。而在实体瘤领域,由于肿瘤微环境复杂、靶点异质性强等原因,CAR-T疗法仍面临诸多挑战,是全球科研界和像元初生物这样的创新企业努力攻坚的方向。
风险与管控:关注细胞治疗的安全性
任何创新疗法都需严格评估其安全性。对于CAR-T细胞治疗,其特有的安全性问题需要临床医生高度重视和妥善管理。
最常见且需要密切关注的不良反应是细胞因子释放综合征(CRS,常被称为“细胞因子风暴”)和可能的神经毒性。CRS是由于大量被激活的CAR-T细胞在体内迅速发挥作用,释放大量炎症因子,引发全身性炎症反应,患者可能出现高热、低血压、呼吸困难等症状,严重时可危及生命。
此外,靶向/脱靶毒性等也是需要监控的风险。因此,开展细胞治疗的医疗机构必须具备处理这些急症不良反应的完备设施和应急预案。令人欣慰的是,国内医学界已积极行动起来,相关学会正组织专家制定临床管理路径指导原则,以规范治疗,保障患者安全。
湖南元初生物认为,国内首款细胞治疗产品的上市是一个里程碑式的事件。它开启了国内细胞治疗产业化的新篇章,但前方的道路依然漫长。从降低生产成本、优化工艺、开发更安全有效的新靶点与新结构,到探索在更多疾病领域的应用,都需要产业界、学术界和医疗界携手共进。元初生物将持续投入研发资源,致力于推动细胞与基因治疗技术的进步,期盼未来能以更可及的方式,惠及广大患者。